नाइट्रोजन परमाणु में इलेक्ट्रॉन होते है जिनका विन्यास निम्न होता है :
`N = 7 " " 1s^(2)2s^(2)2p_(x)^(1) 2p_(y)^(1) 2p_(z)^(1)` (सामान्य अवस्था में)
`1s^(2)2s^(2)2p_(x)^(1) 2p_(y)^(1) 2p_(z)^(1)` (`sp^(3)` संकरित अवस्था में)
N परमाणु `sp^(3)` संकरित अवस्था में होता है। `sp^(3)` संकरित ओर्बिटलो में से एक में युग्मित और तीन में अयुग्मित इलेक्ट्रॉन होते है। अयुग्मित इलेक्ट्रॉन वाली तीन ओर्बिटले , हाइड्रोजन परमाणुओं कि 1s ऑर्बिटल के साथ समाक्ष अतिव्यापन करके `sigma-`बन्ध बनाती है।
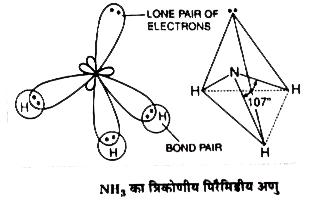
VSEPR सिद्धान्त के अनुसार , युग्मित इलेक्ट्रॉन वाली (lp) ओर्बिटले , बन्ध इलेक्ट्रॉन युग्म (bp) वाली ओर्बिटलो को प्रबलता से प्रतिकर्षित करती है। फलस्वरूप H-N-H कोण का मान `109^(@)28'` से घटकर लगभग `107^(@)45'` हो जाता है और अणु कि ज्यामिति चतुष्फलकीय न होकर त्रिकोणीय पिरैमिडी हो जाती है।
