पदार्थ की विभिन्न अवस्थाओं के गुणों की व्याख्या कीजिए।
पदार्थ की विभिन्न अवस्थाओं के गुणों की व्याख्या कीजिए।
लिखित उत्तर
Verified by Experts
पदार्थ की ठोस, द्रव तथा गैस अवस्था के गुण-धर्म निम्न प्रकार हैं
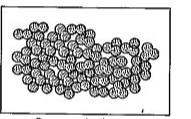
पदार्थ की ठोस अवस्था के गुण-धर्म
ठोस अवस्था के गुण निम्नलिखित हैं
(i) आकार-ठोस अवस्था में, कणों का विन्यास एक निश्चित क्रम के अनुसार होती हैं। कणों के निश्चित स्थानों पर रहने के कारण ठोसों का आकार निश्चित रहता है।
(ii) आयतन-ठोस पर दाब डालने पर उसके आयतन में परिवर्तन नहीं होता क्योंकि उसके कण पास-पास स्थित होते हैं तथा उनकी स्थितियाँ निश्चित होती हैं, अत: ठोस का आयतन भी निश्चित होता है। गर्म करने पर इसके आयतन में उपेक्षणीय अन्तर होता है।
(iii) आकर्षण बल-कण अत्यधिक पास-पास स्थित होते हैं जिससे कणों के बीच अन्तरा-अणुक स्थान बहुत ही कम होते हैं। इनमें पारस्परिक आकर्षण बल भी बहुत शक्तिशाली होता है।
(iv) घनत्व-कणों के परस्पर अत्यधिक निकट होने के कारण ठोस का घनत्व अधिक होता है और यही कारण है कि ठोस कठोर और दृढ़ होते हैं।
(v) गलन—ठोस को गर्म करने पर उसके कणों का अपनी स्थिर स्थिति के इधर-उधर कम्पन बढ़ने लगता है। एक विशेष ताप पर पहुँचकर कण इतने गतिशील हो जाते हैं कि उनका आपसी संसंजक बल उन्हें स्थिर स्थिति में नहीं रख पाता है। इसके फलस्वरूप कण अलग-अलग होकर स्वतन्त्र घूमने लगते हैं। अत: ठोस, द्रव का रूप धारण कर लेता है। ठोस से पिघलकर द्रव बनने की इस क्रिया को गलन (melting) कहते हैं तथा जिस ताप पर ठोस पिघलकर द्रव बनता है, उसे गलनांक (melting point) कहते हैं। पदार्थ की द्रव अवस्था के गुण-धर्म द्रव अवस्था में कणों के मध्य की दूरी ठोस की अपेक्षा कुछ अधिक होती है जिसके फलस्वरूप संसंजक बल कुछ कम होता है। इसी कारण द्रव के कण गति करने के लिए स्वतन्त्र रहते हैं।
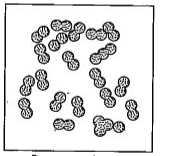
पदार्थ की द्रव अवस्था के गुण निम्नलिखित हैं
(i) आकार-द्रवों के कण गति करते रहते हैं, जिसके फलस्वरूप इनके स्थान स्थिर - नहीं रहते हैं। इसलिए द्रवों के आकार निश्चित नहीं होते हैं।
(ii) आयतन-द्रवों के कण द्रव की सीमा के अन्दर ही स्वतन्त्रतापूर्वक गति करते हैं, किन्तु वे उसके ऊपरी पृष्ठ को नहीं छोड़ पाते हैं। जब कोई अणु द्रव की ऊपरी सतह पर पहुँचता है,तो द्रव के अन्दर के कण उसे आकर्षित करते हैं। फलत: कण द्रव की ऊपरी सतह को भेदकर बाहर नहीं जा पाता है। यही कारण है कि द्रवों का आयतन निश्चित होता है।
(iii) तरलता-द्रव कणों की गतिशीलता के कारण ही तरल होते हैं। द्रव की तरलता उसके कणों के संसंजक बल पर निर्भर करती है। गाढ़े द्रवों में कण कम गतिशील तथा तरल द्रवों में कण अधिक गतिशील होते हैं।
(iv) वाष्पन-द्रव में उसके कण विभिन्न वेगों से गतिमान रहते हुए आपस में टकराते द्रव के कण। रहते हैं, अतः सभी कणों की गतिज ऊर्जा एक-सी नहीं होती। कुछ कणों की गतिज ऊर्जा इतनी बढ़ जाती है कि वे द्रव के तल को छोड़कर वाष्प में बदल जाते हैं। कणों के अधिक गतिमान होने के कारण द्रव से वाष्प अवस्था में बदलने की इस क्रिया को वाष्पन कहते हैं।
(v) क्वथन-द्रव को गर्म करने पर उसके कणों की गतिज ऊर्जा में तेजी से वृद्धि होती है। फलत: तेज गति वाले कण द्रव की सतह को तेजी से छोड़कर वायुमण्डल में आ जाते हैं। द्रव को गर्म करते रहने पर एक स्थिति ऐसी आती है, जब वाष्पन की क्रिया न केवल सतह पर बल्कि पूरे द्रव में होने लगती है, बुलबुले उठने लगते हैं तथा द्रव उबलने लगता है। इस स्थिति में द्रव के सभी कणों की ऊर्जा इतनी हो जाती है कि वे सभी समूहों के रूप में द्रव की सतह को छोड़कर जाने लगते हैं। इस क्रिया को क्वथन या उबलना (boiling) कहते हैं। प्रत्येक द्रव में यह क्रिया एक निश्चित ताप पर होती है, जिसे द्रव का क्वथनांक (boilingpoint) कहा जाता है।
(vi) जमना तथा हिमांक-द्रव को ठण्डा करने पर उसके कणों का वेग कम होने लगता है। एक निश्चित ताप पर इस वेग में इतनी कमी आ जाती है कि अन्तरा-अणुक आकर्षण बल गति को नियन्त्रित कर लेता है और कणों की स्थितियाँ निश्चित होने लगती हैं। फलस्वरूप कण अत्यधिक समीप आ जाते हैं तथा अन्तरा-अणुक स्थान कम हो जाता है। यह जमने की प्रक्रिया है तथा द्रव, ठोस अवस्था में परिवर्तित होने लगता है। किसी द्रव का हिमांक, वह निश्चित ताप है जिस पर उसकी द्रव एवं ठोस अवस्थाओं का वाष्प दाब बराबर हो जाता है।
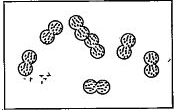
पदार्थ की गैस अवस्था में गुण-धर्म
गैसीय अवस्था में पदार्थ के कण बहुत तेजी से गतिमानं रहते हैं। इनकी गतिज ऊर्जा बहुत अधिक होती है। कणों के मध्य आकर्षण-प्रतिकर्षण बलों के प्रायः ने के कारण स्थितिज ऊर्जा, गतिज ऊर्जा में बदल जाती है तथा कण प्रत्येक दिशा में स्वतन्त्र रूप में गतिशील रहता है। गैस अवस्था के गुण निम्नलिखित हैं
(i) आकार-गैसों के कण गतिशील अवस्था में रहते हैं अर्थात् उनके स्थान स्थिर - नहीं होते हैं। इसलिए गैसों के आकार अनिश्चित होते हैं। जिस भी पात्र में गैस भरी जाती है, उसमें पूर्णतया समान रूप से फैल जाती है तथा उसी का आकार धारण कर लेती है।
(ii) आयतन-गैसों के कण स्वतन्त्रतापूर्वक तीव्र वेग से अनियमित पथ पर सभी सम्भव दिशाओं में निरन्तर गति करते रहते हैं। इसलिए गैसों का आयतन निश्चित नहीं होता है।
(iii) दाब-गैस के कण परस्पर तथा बर्तन की दीवारों से निरन्तर टकराते रहते हैं, .जिससे वेग और दिशा में परिवर्तन होता रहता है। बर्तन की दीवार पर कणों के निरन्तर टकराने के दौरान कण बर्तन की दीवारों को संवेग स्थानान्तरित करते हैं और संवेग चित्र गैस के कण! स्थानान्तरण के फलस्वरूप ही गैस दाब उत्पन्न होता है।
(iv) गतिज ऊर्जा-गैसीय अवस्था में स्थितिज ऊर्जा पूर्णतया गतिज ऊर्जा में बदल जाती है। अत: गैस के कणों की गतिज ऊर्जा पदार्थ की शेष अवस्थाओं में सर्वाधिक होती है।
(v) द्रवण-गैस पर दाब लगाने एवं उसका ताप कम करने पर अणु पास-पास आते हैं तथा उनकी गति मन्द होती जाती है। इस प्रकार दाब लगाकर गैस को ठण्डा करने पर वह द्रव में बदल जाती है। गैस के द्रव बनने की इस क्रिया को द्रवण कहते हैं।

पदार्थ की ठोस अवस्था के गुण-धर्म
ठोस अवस्था के गुण निम्नलिखित हैं
(i) आकार-ठोस अवस्था में, कणों का विन्यास एक निश्चित क्रम के अनुसार होती हैं। कणों के निश्चित स्थानों पर रहने के कारण ठोसों का आकार निश्चित रहता है।
(ii) आयतन-ठोस पर दाब डालने पर उसके आयतन में परिवर्तन नहीं होता क्योंकि उसके कण पास-पास स्थित होते हैं तथा उनकी स्थितियाँ निश्चित होती हैं, अत: ठोस का आयतन भी निश्चित होता है। गर्म करने पर इसके आयतन में उपेक्षणीय अन्तर होता है।
(iii) आकर्षण बल-कण अत्यधिक पास-पास स्थित होते हैं जिससे कणों के बीच अन्तरा-अणुक स्थान बहुत ही कम होते हैं। इनमें पारस्परिक आकर्षण बल भी बहुत शक्तिशाली होता है।
(iv) घनत्व-कणों के परस्पर अत्यधिक निकट होने के कारण ठोस का घनत्व अधिक होता है और यही कारण है कि ठोस कठोर और दृढ़ होते हैं।
(v) गलन—ठोस को गर्म करने पर उसके कणों का अपनी स्थिर स्थिति के इधर-उधर कम्पन बढ़ने लगता है। एक विशेष ताप पर पहुँचकर कण इतने गतिशील हो जाते हैं कि उनका आपसी संसंजक बल उन्हें स्थिर स्थिति में नहीं रख पाता है। इसके फलस्वरूप कण अलग-अलग होकर स्वतन्त्र घूमने लगते हैं। अत: ठोस, द्रव का रूप धारण कर लेता है। ठोस से पिघलकर द्रव बनने की इस क्रिया को गलन (melting) कहते हैं तथा जिस ताप पर ठोस पिघलकर द्रव बनता है, उसे गलनांक (melting point) कहते हैं। पदार्थ की द्रव अवस्था के गुण-धर्म द्रव अवस्था में कणों के मध्य की दूरी ठोस की अपेक्षा कुछ अधिक होती है जिसके फलस्वरूप संसंजक बल कुछ कम होता है। इसी कारण द्रव के कण गति करने के लिए स्वतन्त्र रहते हैं।

पदार्थ की द्रव अवस्था के गुण निम्नलिखित हैं
(i) आकार-द्रवों के कण गति करते रहते हैं, जिसके फलस्वरूप इनके स्थान स्थिर - नहीं रहते हैं। इसलिए द्रवों के आकार निश्चित नहीं होते हैं।
(ii) आयतन-द्रवों के कण द्रव की सीमा के अन्दर ही स्वतन्त्रतापूर्वक गति करते हैं, किन्तु वे उसके ऊपरी पृष्ठ को नहीं छोड़ पाते हैं। जब कोई अणु द्रव की ऊपरी सतह पर पहुँचता है,तो द्रव के अन्दर के कण उसे आकर्षित करते हैं। फलत: कण द्रव की ऊपरी सतह को भेदकर बाहर नहीं जा पाता है। यही कारण है कि द्रवों का आयतन निश्चित होता है।
(iii) तरलता-द्रव कणों की गतिशीलता के कारण ही तरल होते हैं। द्रव की तरलता उसके कणों के संसंजक बल पर निर्भर करती है। गाढ़े द्रवों में कण कम गतिशील तथा तरल द्रवों में कण अधिक गतिशील होते हैं।
(iv) वाष्पन-द्रव में उसके कण विभिन्न वेगों से गतिमान रहते हुए आपस में टकराते द्रव के कण। रहते हैं, अतः सभी कणों की गतिज ऊर्जा एक-सी नहीं होती। कुछ कणों की गतिज ऊर्जा इतनी बढ़ जाती है कि वे द्रव के तल को छोड़कर वाष्प में बदल जाते हैं। कणों के अधिक गतिमान होने के कारण द्रव से वाष्प अवस्था में बदलने की इस क्रिया को वाष्पन कहते हैं।
(v) क्वथन-द्रव को गर्म करने पर उसके कणों की गतिज ऊर्जा में तेजी से वृद्धि होती है। फलत: तेज गति वाले कण द्रव की सतह को तेजी से छोड़कर वायुमण्डल में आ जाते हैं। द्रव को गर्म करते रहने पर एक स्थिति ऐसी आती है, जब वाष्पन की क्रिया न केवल सतह पर बल्कि पूरे द्रव में होने लगती है, बुलबुले उठने लगते हैं तथा द्रव उबलने लगता है। इस स्थिति में द्रव के सभी कणों की ऊर्जा इतनी हो जाती है कि वे सभी समूहों के रूप में द्रव की सतह को छोड़कर जाने लगते हैं। इस क्रिया को क्वथन या उबलना (boiling) कहते हैं। प्रत्येक द्रव में यह क्रिया एक निश्चित ताप पर होती है, जिसे द्रव का क्वथनांक (boilingpoint) कहा जाता है।
(vi) जमना तथा हिमांक-द्रव को ठण्डा करने पर उसके कणों का वेग कम होने लगता है। एक निश्चित ताप पर इस वेग में इतनी कमी आ जाती है कि अन्तरा-अणुक आकर्षण बल गति को नियन्त्रित कर लेता है और कणों की स्थितियाँ निश्चित होने लगती हैं। फलस्वरूप कण अत्यधिक समीप आ जाते हैं तथा अन्तरा-अणुक स्थान कम हो जाता है। यह जमने की प्रक्रिया है तथा द्रव, ठोस अवस्था में परिवर्तित होने लगता है। किसी द्रव का हिमांक, वह निश्चित ताप है जिस पर उसकी द्रव एवं ठोस अवस्थाओं का वाष्प दाब बराबर हो जाता है।
पदार्थ की गैस अवस्था में गुण-धर्म
गैसीय अवस्था में पदार्थ के कण बहुत तेजी से गतिमानं रहते हैं। इनकी गतिज ऊर्जा बहुत अधिक होती है। कणों के मध्य आकर्षण-प्रतिकर्षण बलों के प्रायः ने के कारण स्थितिज ऊर्जा, गतिज ऊर्जा में बदल जाती है तथा कण प्रत्येक दिशा में स्वतन्त्र रूप में गतिशील रहता है। गैस अवस्था के गुण निम्नलिखित हैं
(i) आकार-गैसों के कण गतिशील अवस्था में रहते हैं अर्थात् उनके स्थान स्थिर - नहीं होते हैं। इसलिए गैसों के आकार अनिश्चित होते हैं। जिस भी पात्र में गैस भरी जाती है, उसमें पूर्णतया समान रूप से फैल जाती है तथा उसी का आकार धारण कर लेती है।
(ii) आयतन-गैसों के कण स्वतन्त्रतापूर्वक तीव्र वेग से अनियमित पथ पर सभी सम्भव दिशाओं में निरन्तर गति करते रहते हैं। इसलिए गैसों का आयतन निश्चित नहीं होता है।
(iii) दाब-गैस के कण परस्पर तथा बर्तन की दीवारों से निरन्तर टकराते रहते हैं, .जिससे वेग और दिशा में परिवर्तन होता रहता है। बर्तन की दीवार पर कणों के निरन्तर टकराने के दौरान कण बर्तन की दीवारों को संवेग स्थानान्तरित करते हैं और संवेग चित्र गैस के कण! स्थानान्तरण के फलस्वरूप ही गैस दाब उत्पन्न होता है।
(iv) गतिज ऊर्जा-गैसीय अवस्था में स्थितिज ऊर्जा पूर्णतया गतिज ऊर्जा में बदल जाती है। अत: गैस के कणों की गतिज ऊर्जा पदार्थ की शेष अवस्थाओं में सर्वाधिक होती है।
(v) द्रवण-गैस पर दाब लगाने एवं उसका ताप कम करने पर अणु पास-पास आते हैं तथा उनकी गति मन्द होती जाती है। इस प्रकार दाब लगाकर गैस को ठण्डा करने पर वह द्रव में बदल जाती है। गैस के द्रव बनने की इस क्रिया को द्रवण कहते हैं।

Recommended Questions
- पदार्थ की विभिन्न अवस्थाओं के गुणों की व्याख्या कीजिए।
Text Solution
|
- पदार्थ की अवस्थाओं का पारस्परिक परिवर्तन
Text Solution
|
- पदार्थ का वर्गीकरण||पदार्थ के भौतिक गुणों पर आधारित वर्गीकरण
Text Solution
|
- पदार्थ की अवस्थाओं का पारस्परिक परिवर्तन
Text Solution
|
- कविता के आधार पर 'मनुष्यता' के गुणों/लक्षणों की चर्चा विस्तारपूर्वक की...
Text Solution
|
- सीखिए पदार्थ की भौतिक अवस्थाओं में परिवर्तन
Text Solution
|
- वसंत - रहीम के दोहे | दोहे | रहीम के दोहे की व्याख्या
Text Solution
|
- Exam Special|गति के समीकरण की व्याख्या
Text Solution
|
- द्रव्य के तापीय गुण|पदार्थ की गुप्त ऊष्मा #!#गुप्त ऊष्मा की अणुगति सिद...
Text Solution
|