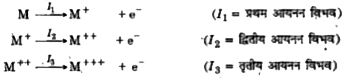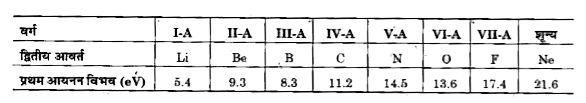आयनन विभव (Ionization Potential) आयनन ऊर्जा—किसी तत्व के एक विलग (isolated) गैसीय परमाणु की तलस्थ अवस्था में उसकी बाह्यतम कोश से एक इलेक्ट्रॉन पृथक करने के लिए जितनी ऊर्जा की आवश्यकता होती है, उसे उस तत्व का आयनन विभव (आयनन ऊर्जा) या प्रथम आयनन विभव कहते हैं। इसी प्रकार, दूसरे तथा तीसरे इलेक्ट्रॉनों को बाहर निकालने के लिए प्रयुक्त ऊर्जा को क्रमशः द्वितीय आयनन विभव तथा तृतीय आयनन विभव कहते हैं।
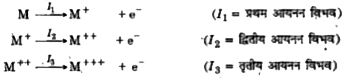
आयनन विभव को इलेक्ट्रॉन-वोल्ट (eV) या किलोकैलोरी प्रति मोल (kcal/mol) या किलोजूल प्रति मोल (kJ/mol) में व्यक्त करते हैं। (इनमें क्रम. `I_1 lt I_2 ltI_3 lt...`) .
आवर्त में-किसी आवर्त में बाएँ से दाएँ जाने पर अर्थात् परमाणु क्रमांक में वृद्धि से नाभिकीय आवेश में वृद्धि होती है और परमाणु का आकार कम होने लगता है, जिसके कारण बाह्यतम, कोश से इलेक्ट्रॉनों का नाभिक के प्रति आकर्षण बढ़ता है, फलस्वरूप बाह्यतम कोश से इलेक्ट्रॉन पृथक् करने हेतु आवश्यक ऊर्जा का मान बढ़ता जाता है। अत: आयनन विभव बढ़ता है
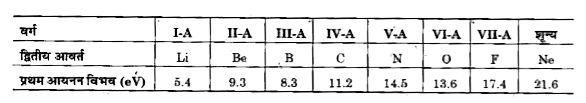
वर्ग में किसी वर्ग में ऊपर से नीचे जाने पर अर्थात् परमाणु क्रमांक में वृद्धि के साथ इनके परमाणु आकार में वृद्धि होती है, जिससे नाभिकीय आवेश का बाहरी कोश के इलेक्ट्रॉन पर आकर्षण कम हो जाता है और इलेक्ट्रॉनों को निकालने में कम ऊर्जा लगती है, जिससे आयनन विभव का मान कम हो जाता है।