लिखित उत्तर
Verified by Experts
टॉपर्स ने हल किए ये सवाल
परमाणु
PRABODH PUBLICATION|Exercise NCERT पाठ्य पुस्तक के अभ्यासार्थ प्रश्न हल सहित|14 Videosपरमाणु
PRABODH PUBLICATION|Exercise अतिरिक्त प्रश्न|10 Videosपरमाणु
PRABODH PUBLICATION|Exercise आंकिक प्रश्न|15 Videosनाभिक
PRABODH PUBLICATION|Exercise मूल्य आधारित प्रश्न|8 Videosप्रत्यावर्ती धारा
PRABODH PUBLICATION|Exercise आंकिक प्रश्न|15 Videos
PRABODH PUBLICATION-परमाणु -दीर्घ उत्तरीय प्रश्न
- रदरफोर्ड के alpha - प्रकीर्णन प्रयोग की सचित्र व्याख्या कीजिए । रदरफोर...
Text Solution
|
- रदरफोर्ड परमाणु की उन सीमाओं को लिखिए जो परमाणु स्पेक्ट्रम में अवलोकित...
Text Solution
|
- रदरफोर्ड के परमाणु मॉडल की सहायता से हाइड्रोजन परमाणु के इलेक्ट्रॉन की...
Text Solution
|
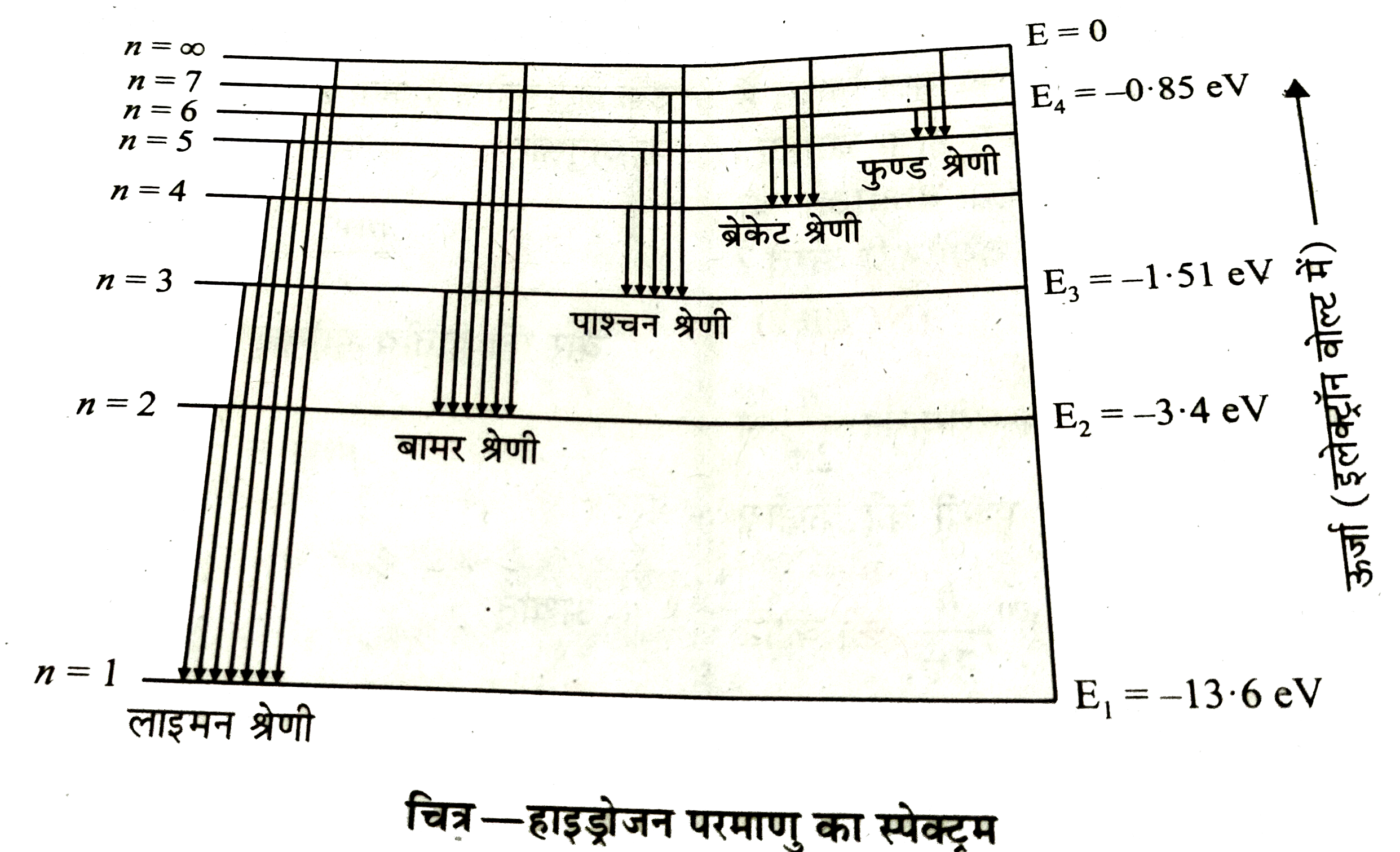
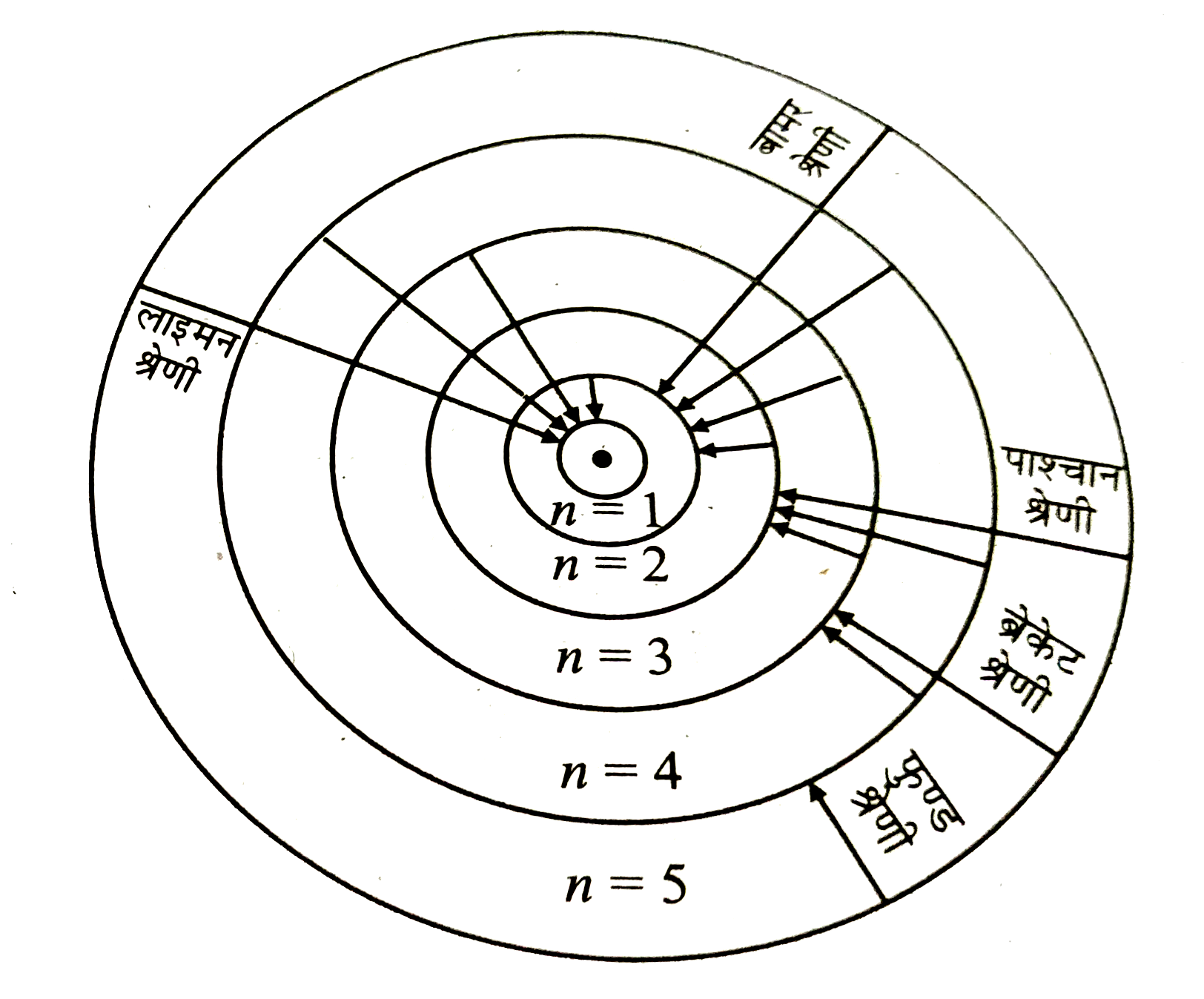
- परमाणु का ऊर्जा स्तर क्या हैं ? हाइड्रोजन परमाणु के विभिन्न ऊर्जा स्तर...
Text Solution
|
- बोर के अभिगृहीत को लिखिए तथा हाइड्रोजन परमाणु में जब इलेक्ट्रॉन उच्च ऊ...
Text Solution
|
- सिद्ध कीजिए कि परमाणु में स्थायी कक्षाओं की त्रिज्याओं का अनुपात 1 : 4...
Text Solution
|
- हाइड्रोजन स्पेक्ट्रम की विभिन्न श्रेणियों को एक ऊर्जा स्तर आरेख द्वारा...
Text Solution
|
- स्पेक्ट्रमी श्रेणी किसे कहते है? बामर श्रेणी को परिभाषित करते हुए इसकी...
Text Solution
|
- बोर मॉडल की मूल परिकल्पनायें लिखिए। n वी कक्षा में स्थायी कक्षा में इल...
Text Solution
|